Les définitions
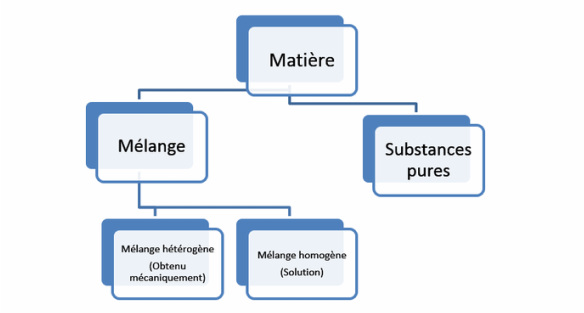
a) Substance pure:
Une substance pure contient un seul type de particule. Il existe beaucoup de substances pures, mais quelques-unes seulement se retrouvent dans la nature. Une substance pure peut ainsi être défini "n'importe quelle matière avec une composition chimique définie".
Pour purifier ces substances, nous prenons le matériau brut qui les contient, et en séparons la substance désirée.
Exemple :
Matériau brut Substance pure
Betterave à sucre + canne à sucre à sucre de table
Bauxite à Papier d’aluminium
Attention : Nous pensons souvent que notre eau potable est pure, mais cette eau contient des produits chimiques pour éliminer les bactéries, et elle est donc, constituée de plusieurs substances chimiques.
Toutefois, chaque substance qui se trouve dans l'eau garde ses propriétés chimiques qui leurs appartiennent, alors quand tu as bouilli l'eau, ses substances dissouts resteront. Quand l'eau est un substance pure, on l'apelle l'eau distillé; il contient seulement des molécules d'eau dedans--l'Hydrogène et Oxygène.
Pour purifier ces substances, nous prenons le matériau brut qui les contient, et en séparons la substance désirée.
Exemple :
Matériau brut Substance pure
Betterave à sucre + canne à sucre à sucre de table
Bauxite à Papier d’aluminium
Attention : Nous pensons souvent que notre eau potable est pure, mais cette eau contient des produits chimiques pour éliminer les bactéries, et elle est donc, constituée de plusieurs substances chimiques.
Toutefois, chaque substance qui se trouve dans l'eau garde ses propriétés chimiques qui leurs appartiennent, alors quand tu as bouilli l'eau, ses substances dissouts resteront. Quand l'eau est un substance pure, on l'apelle l'eau distillé; il contient seulement des molécules d'eau dedans--l'Hydrogène et Oxygène.
b) Les mélanges :
Un mélange contient deux ou plusieurs substances pures. Tout comme les produits fabriqués ou manufacturés par les humains, presque toutes les substances naturelles dans le monde sont des mélanges de substances pures. Il y a une nombre infinite de mélanges, tout ce qui peut être combiné est un mélange. Un mélange c'est une combinaison de deux ou plus composants distincts réuni dans une récipant.
Les mélanges peuvent être n’importe quelle combinaison de solides, de liquides ou de gaz.
Exemple:
1. Les boissons gazeuses sont un mélange contenant de l’eau à l’état liquide et du sucre à l’état solide et du dioxyde de carbone à l’état gazeux.
2. Le pain est un mélange de levure, de farine, de sucre, d’eau d’air et d’autres produits chimiques.
c) Mélanges hétérogènes et homogènes:
- Hétérogène signifie « plusieurs types ». Deux ou plusieurs substances distinctes peuvent être vues et touchées dans un mélange hétérogène. Les substances ne sont pas mélangés uniformements, donc on peut en distinguer les différents composants. Ils peuvent être vus ou touchés, ou les deux.
Si tu prends un petit échantillon d’un mélange hétérogène, il pourra avoir des propriétés différentes de celles d’un autre échantillon. Un mélange hétérogène se nomme aussi mélange obtenu mécaniquement.
-Homogène signifie « de même type ». Les particules pures se mélangent uniformément, de sorte que le mélange a l’apparence et l’aspect d’une seule et même substance. Les substances différents ne se distinguent plus. Peu importe la taille de ton échantillon, les propriétés de ce mélange sont toujours les mêmes.
Exemple :
-L’acier, composé de fer, d’oxygène et de carbone, est un mélange homogène. Peu importe ou tu coupes dans un bar d’acier, elle sera toujours la même.
-Lorsque tu mélanges une petit quantité de sel avec l’eau, tu créés un mélange homogène, qu’on appelle aussi une solution.
d) La sursaturation:
Il est possible de créer une solution qui est plus que saturée. On nomme sursaturation une solution qui contient plus de soluté que la quantité qui est présente dans une solution saturée.
Avec les solutions sursaturées, le soluté ne se dissoudra ou mélangera pas dans le solvant. Il se déposera simplement au fond puisque tout les espaces disponibles entre les particules du solvant sont remplis.
Avec les solutions sursaturées, le soluté ne se dissoudra ou mélangera pas dans le solvant. Il se déposera simplement au fond puisque tout les espaces disponibles entre les particules du solvant sont remplis.
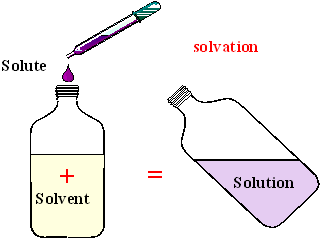
e) Solvant
Le mot solvant signifie "composé le plus abondant (eau en biologie)". Il vient du mot latin "solvō", "Je délie, je détache," ou "je résoudre".
Les solvants sont des substances ont la propriété de dissoudre, de diluer ou d'extraire d’autres substances sans les modifier chimiquement ni modifier lui-même.
La soluté se dissout dans le solvant, se qui créé une solution. Il est souvent une liquide, mais peut aussi être une gaz, ou solide.
Les solvants organiques sont souvent utilisés dans le nettoyage (vêtements, verinis à ongles, etc.). Un exemple c'est la térébenthine, un solvant utilisé pour nettoyer (dissoudre) les peintures à base d'huile sur les pinceaux. Les solvants sont utilisés dans plusieurs produits, tels le dégraissage, les peintures, les encres, la détergence, la synthèse organique, et représentent des quantités considérables.
Les solvants sont des substances ont la propriété de dissoudre, de diluer ou d'extraire d’autres substances sans les modifier chimiquement ni modifier lui-même.
La soluté se dissout dans le solvant, se qui créé une solution. Il est souvent une liquide, mais peut aussi être une gaz, ou solide.
Les solvants organiques sont souvent utilisés dans le nettoyage (vêtements, verinis à ongles, etc.). Un exemple c'est la térébenthine, un solvant utilisé pour nettoyer (dissoudre) les peintures à base d'huile sur les pinceaux. Les solvants sont utilisés dans plusieurs produits, tels le dégraissage, les peintures, les encres, la détergence, la synthèse organique, et représentent des quantités considérables.
f) Soluté
Le soluté est l'espèce minoritaire dans une solution. Il est dissous par le solvant.
Par exemple, le sel est le soluté dans une solution d'eau salée.
Il y a 2 types différentes de solutés :
1. Les cristalloïdes:
Par exemple, le sel est le soluté dans une solution d'eau salée.
Il y a 2 types différentes de solutés :
1. Les cristalloïdes:
- Les cristalloides contiennent des particules de petites tailles (sels minéraux, glucose) qui sortent rapidement des vaisseaux et passe dans le liquide interstitiel. Leur effet est lié à leur osmolalité (mesure du nombre d'osmoles de soluté par kilogramme de solvant).
- Cette type de soluté contiennent des grosses molécules qui restent dans les vaisseaux pendant un certain temps et attirent l'eau des liquides interstitiels (atomes du liquide qui se trouve dans une structure cristalline lors d'un espace normalement occupé). Leur effet est lié à leur pouvoir oncotique (force qui attire l'eau en direction des protéines).